![Wiązania chemiczne, elektroujemność #1 [ Tworzenie związków chemicznych ]](https://i.ytimg.com/vi/6gDkTPiiKXE/hqdefault.jpg)
Zawartość
W chemii, elektroujemność jest to miara przyciągania, jakie atom wywiera na elektrony w wiązaniu. Atom o wysokiej elektroujemności przyciąga elektrony z dużą intensywnością, podczas gdy atom o niskiej elektroujemności będzie to robił z małą intensywnością. Wartości te są używane do przewidywania, jak różne atomy będą się zachowywać po związaniu ze sobą, co sprawia, że ten temat jest ważną umiejętnością w podstawowej chemii.
Kroki
Metoda 1 z 3: Podstawowe pojęcia o elektroujemności
Zrozum, że wiązania chemiczne zachodzą, gdy atomy mają wspólne elektrony. Aby zrozumieć elektroujemność, należy najpierw zrozumieć, czym jest „łącze”. Mówi się, że dowolne dwa atomy w cząsteczce „połączone” ze sobą na schemacie molekularnym mają między sobą wiązanie. Zasadniczo oznacza to, że mają wspólny zestaw dwóch elektronów - każdy atom wnosi atom do wiązania.
- Dokładne powody, dla których atomy dzielą elektrony i wiążą się ze sobą, nie odpowiadają tematowi tego artykułu. Jeśli chcesz dowiedzieć się więcej, poszukaj w Internecie podstawowych pojęć dotyczących wiązań chemicznych.
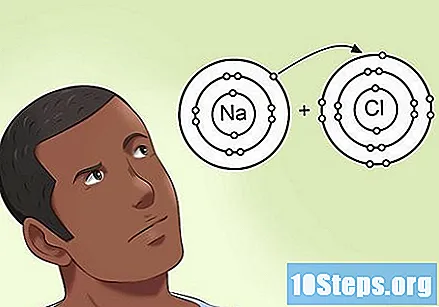
Dowiedz się, jak elektroujemność wpływa na elektrony obecne w wiązaniu. Kiedy dwa atomy mają wspólny zestaw dwóch elektronów w wiązaniu, nie zawsze istnieje równy podział między nimi. Kiedy jeden z nich ma wyższą elektroujemność niż atom, do którego jest przyłączony, zbliża dwa elektrony do siebie. Atom o bardzo wysokiej elektroujemności może przyciągać elektrony na bok w wiązaniu, prawie anulując ich współdzielenie.- Na przykład w cząsteczce NaCl (chlorku sodu) atom chloru ma wysoką elektroujemność, a sód niską elektroujemność. Wkrótce elektrony zostaną wyciągnięte w kierunku chloru i z dala od sodu.

Użyj tabeli elektroujemności jako odniesienia. Tablica elektroujemności przedstawia pierwiastki ułożone dokładnie tak, jak w układzie okresowym, ale z każdym atomem oznaczonym elektroujemnością. Można je znaleźć w kilku podręcznikach chemii, w artykułach technicznych, a także w Internecie.- Oto doskonała tabela elektroujemności. Zauważ, że używa skali elektroujemności Paulinga, która jest bardziej powszechna. Istnieją jednak inne sposoby pomiaru elektroujemności, z których jeden zostanie pokazany poniżej.
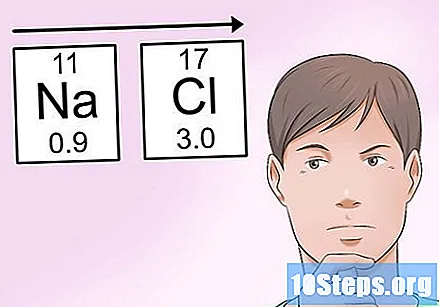
Zapamiętaj trendy elektroujemności, aby łatwo oszacować. Jeśli nie masz pod ręką tabeli elektroujemności, nadal możesz oszacować tę wartość na podstawie swojej lokalizacji w układzie okresowym. Z reguły:- Elektroujemność atomu wzrasta kiedy przejdziesz do dobrze w układzie okresowym pierwiastków.
- Elektroujemność atomu wzrasta jak się przenosisz w górę w układzie okresowym pierwiastków.
- Dlatego atomy w prawym górnym rogu mają najwyższe wartości elektroujemności, a atomy w lewym dolnym rogu mają najniższe.
- Na przykład w poprzednim przykładzie NaCl można określić, że chlor ma wyższą elektroujemność niż sód, ponieważ znajduje się prawie w najwyższym prawym punkcie. Z drugiej strony sód znajduje się daleko na lewo od tabeli, co czyni go jednym z najmniej wartościowych atomów.
Metoda 2 z 3: Znajdowanie powiązań z elektroujemnością
Znajdź różnicę w elektroujemności między dwoma atomami. Kiedy dwa atomy są ze sobą połączone, różnica między ich wartościami elektroujemności wiele mówi o jakości tego wiązania. Odejmij najmniejszą wartość od największej, aby znaleźć różnicę.
- Na przykład, jeśli patrzymy na cząsteczkę HF, odejmiemy wartość elektroujemności wodoru (2,1) od fluoru (4,0). 4,0 - 2,1 = 1,9.
Jeśli różnica jest poniżej 0,5, wiązanie jest kowalencyjne i niepolarne. Tutaj elektrony są dzielone prawie w równym stopniu. Te wiązania nie tworzą cząsteczek o dużych różnicach ładunku na obu końcach. Wiązania biegunowe są często bardzo trudne do zerwania.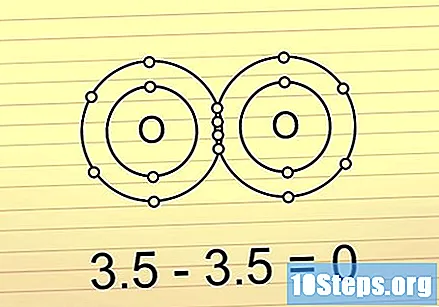
- Na przykład cząsteczka O2 przedstawia ten typ połączenia. Ponieważ dwie cząsteczki tlenu mają taką samą elektroujemność, różnica między nimi jest równa 0.
Jeśli różnica wynosi od 0,5 do 1,6, wiązanie jest kowalencyjne i polarne. Te wiązania zawierają więcej elektronów na jednym końcu niż na drugim. To sprawia, że cząsteczka jest nieco bardziej ujemna na końcu z większą liczbą elektronów i nieco bardziej dodatnia na końcu bez nich. Brak równowagi ładunków w tych wiązaniach pozwala cząsteczkom uczestniczyć w pewnych określonych reakcjach.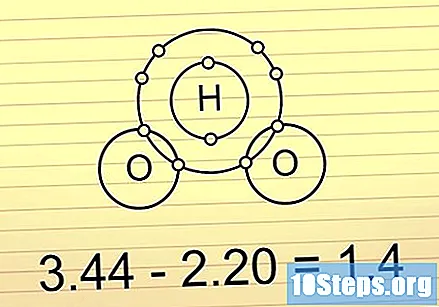
- Dobrym tego przykładem jest cząsteczka H.2O (woda). O jest bardziej elektroujemne niż dwa H, więc utrzymuje elektrony bliżej i sprawia, że cała cząsteczka jest częściowo ujemna na końcu O i częściowo dodatnia na końcach H.
Jeśli różnica jest większa niż 2, wiązanie jest jonowe. W tych wiązaniach elektrony są umieszczone całkowicie na jednym końcu. Najbardziej elektroujemny atom zyskuje ładunek ujemny, a najmniej elektroujemny - dodatni. Ten typ wiązania pozwala atomom reagować z innymi atomami lub, co więcej, oddzielać je atomami polarnymi.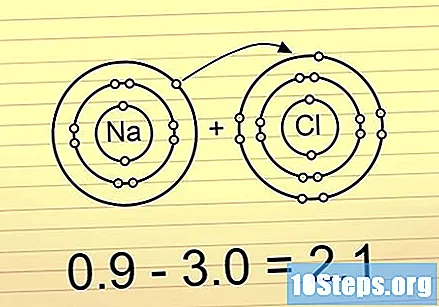
- Przykładem tego jest NaCl (chlorek sodu). Chlor jest tak elektroujemny, że przyciąga oba elektrony z wiązania do siebie, pozostawiając sód z ładunkiem dodatnim.
Jeśli różnica wynosi od 1,6 do 2, poszukaj metalu. Jeśli tam metal obecny w wiązaniu, oznacza to, że tak jest joński. Jeśli istnieją inne niemetale, wiązanie jest polarny kowalencyjny.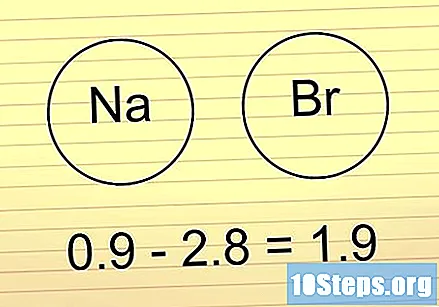
- Metale zawierają większość atomów po lewej stronie i pośrodku układu okresowego. Ta strona zawiera tabelę pokazującą, które elementy są metalami.
- Nasz poprzedni przykład HF należy do tej grupy. Ponieważ H i F nie są metalami, wiązanie będzie polarny kowalencyjny.
Metoda 3 z 3: Odkryj elektroujemność Mullikena
Znajdź pierwszą energię jonizacji swojego atomu. Elektroujemność Mullikena składa się z metody pomiaru nieco innej niż ta, którą można znaleźć w powyższej tabeli Paulinga. Aby znaleźć jego wartość dla danego atomu, znajdź swoją pierwszą energię jonizacji. Jest to energia potrzebna do wyładowania atomu pojedynczego elektronu.
- Wartość tę można prawdopodobnie znaleźć w chemicznych materiałach odniesienia. Na tej stronie znajduje się dobry stół, którego możesz użyć (przewiń w dół, aby go znaleźć).
- Jako przykład, powiedzmy, że chcesz dowiedzieć się, jaka jest elektroujemność litu (Li). W tabeli na powyższej stronie widzimy, że pierwsza energia jonizacji jest równoważna 520 kJ / mol.
Dowiedz się, jakie jest powinowactwo elektronowe atomu. Jest to pomiar energii uzyskanej po dodaniu elektronu do atomu w celu utworzenia jonu ujemnego. Ponownie, jest to coś, co powinno się znaleźć w materiałach referencyjnych. Ta strona zawiera zasoby, które mogą być przydatne.
- Elektroniczne powinowactwo litu jest równe 60 kJ mol.
Rozwiąż równanie elektroujemności Mullikena. Używając kJ / mol jako jednostki energii, równanie elektroujemności Mullikena można zapisać jako ENMulliken = (1,97 × 10) (E.ja + E.i) + 0,19. Wstaw znane dane do równania i znajdź wartość ENMulliken.
- W naszym przykładzie dojdziemy do następującego rozwiązania:
- ENMulliken = (1,97 × 10) (E.ja + E.i) + 0,19
- ENMulliken = (1,97 × 10)(520 + 60) + 0,19
- ENMulliken = 1,143 + 0,19 = 1,333
- W naszym przykładzie dojdziemy do następującego rozwiązania:
Porady
- Oprócz skal Paulinga i Mullikena istnieją inne skale elektroujemności, takie jak Allred-Rochow, Sanderson i Allen. Każdy z nich ma własne równania do obliczania elektroujemności (a niektóre z nich mogą być dość złożone).
- Elektroujemność nie ma jednostki miary.