Zawartość
Chociaż wszystkie atomy tego samego pierwiastka zawierają taką samą liczbę protonów, liczba neutronów może się zmieniać. Wiedza o tym, ile neutronów ma dany atom, może pomóc w określeniu, czy cząstka jest regularna w tym pierwiastku, czy w izotopie, który będzie miał mniej lub więcej neutronów. Określenie liczby neutronów w atomie jest dość proste i nie wymaga żadnego eksperymentu. Aby obliczyć liczbę neutronów w zwykłym atomie lub izotopie, postępuj zgodnie z tymi instrukcjami z układem okresowym w ręku.
Kroki
Metoda 1 z 2: Wyznaczanie liczby cząsteczek neutralnych we wspólnym atomie
Zlokalizuj element w układzie okresowym. W tym przykładzie spójrzmy na system operacyjny (OS), który znajduje się w szóstym rzędzie, od góry do dołu.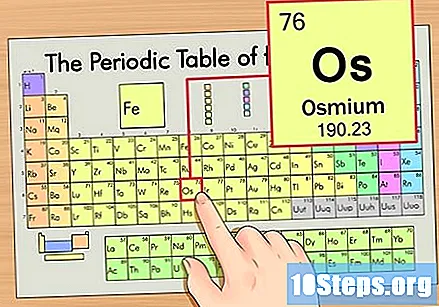
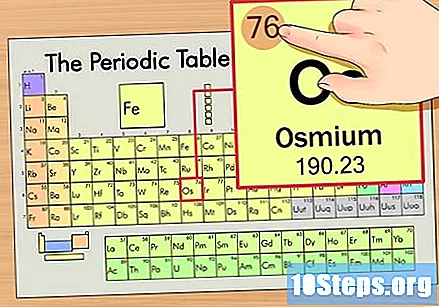
Znajdź liczbę atomową pierwiastka. Zwykle jest to najbardziej widoczna liczba dla danego elementu i zwykle znajduje się nad jego symbolem (w używanej przez nas tabeli w rzeczywistości nie ma innej liczby). Liczba atomowa to liczba protonów w pojedynczym atomie tego pierwiastka. Liczba Os wynosi 76, co oznacza, że atom Osmu ma 76 protonów.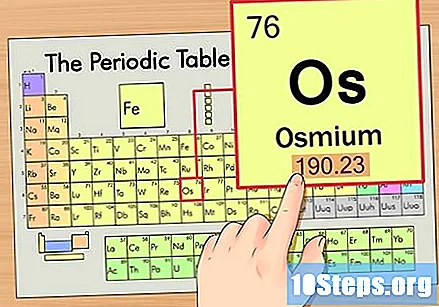
Znajdź masę atomową pierwiastka. Liczba ta znajduje się zwykle pod symbolem atomowym. Zwróć uwagę, że tabela w tym przykładzie jest oparta tylko na liczbie atomowej i nie podaje masy atomowej. Nie zawsze tak będzie. Osm ma masę atomową 190,23.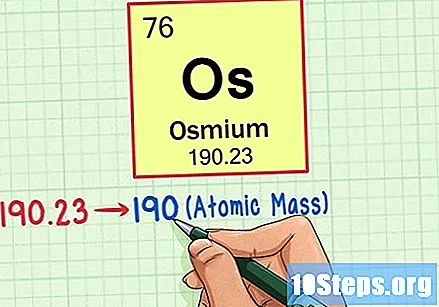
Zaokrąglij masę atomową do najbliższej liczby całkowitej, aby znaleźć masę atomową. W naszym przykładzie 190,23 byłoby zaokrąglone do 190, co daje masę atomową osmu równą 190.- Masa atomowa jest średnią izotopów pierwiastka. Dlatego zwykle nie jest liczbą całkowitą.
Odejmij liczbę atomową od masy atomowej. Ponieważ zdecydowana większość masy atomu znajduje się w jego protonach i substancjach obojętnych, odjęcie liczby protonów (czyli liczby atomowej) od masy atomowej da ci liczbę obliczony neutronów w atomie. Liczba po przecinku oznacza na ogół bardzo małą masę elektronów w atomie. W naszym przykładzie jest to: 190 (masa atomowa) - 76 (liczba protonów) = 114 (liczba neutronów).
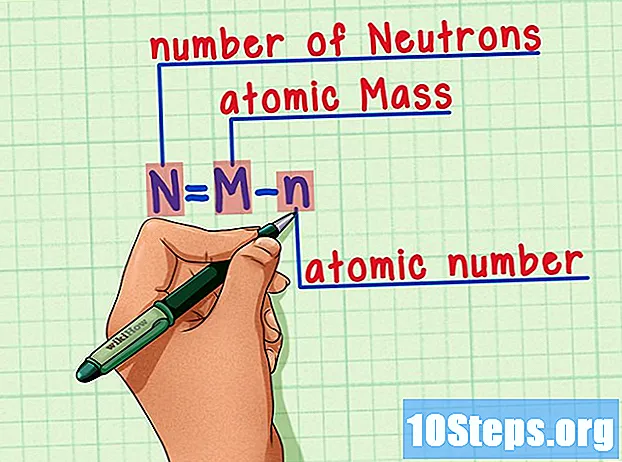
Zapamiętaj wzór. Aby znaleźć liczbę neutronów w przyszłości, użyj tego wzoru: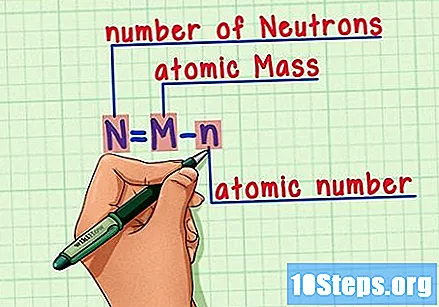
- N = M - n.
- N = liczba Neutrony.
- M = Matomowa pieczeń.
- n = natomowa kość ramienna.
- N = M - n.
Metoda 2 z 2: Wyznaczanie liczby neutronów w izotopie
Zlokalizuj element w układzie okresowym. Na przykład użyjmy izotopu węgla-14. Ponieważ nieizotopową formą węgla-14 jest po prostu węgiel (C), znajdź ten pierwiastek w układzie okresowym (w drugim rzędzie).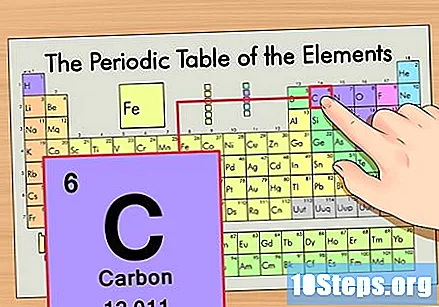
Znajdź liczbę atomową pierwiastka. Zwykle jest to najbardziej widoczna liczba dla danego elementu i zwykle znajduje się nad jego symbolem (w używanej przez nas tabeli w rzeczywistości nie ma innej liczby). Liczba atomowa to liczba protonów w pojedynczym atomie tego pierwiastka. C to liczba 6, co oznacza, że atom węgla ma 6 protonów.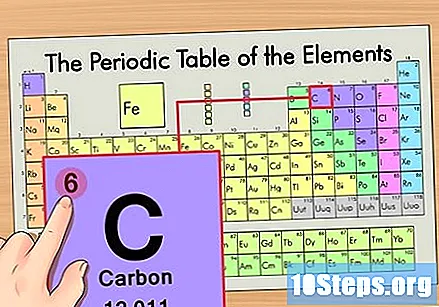
Znajdź masę atomową. Jest to niezwykle łatwe w przypadku izotopów, ponieważ ich nazwy pochodzą od ich masy atomowej. Węgiel-14 ma masę atomową 14. Gdy już znajdziesz masę atomową izotopu, proces znajdowania liczby neutronów jest taki sam, jak w przypadku zwykłych atomów.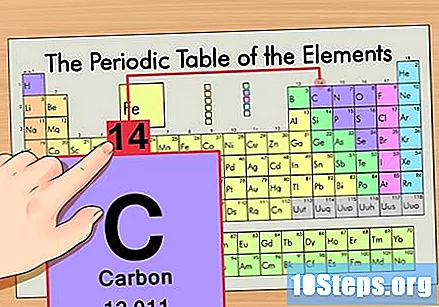
Odejmij liczbę atomową od masy atomowej. Ponieważ zdecydowana większość masy atomu znajduje się w jego protonach i substancjach obojętnych, odjęcie liczby protonów (czyli liczby atomowej) od masy atomowej da ci liczbę obliczony neutronów w atomie. Liczba po przecinku oznacza na ogół bardzo małą masę elektronów w atomie. W naszym przykładzie jest to: 14 (masa atomowa) - 6 (liczba protonów) = 8 (liczba neutronów).
Zapamiętaj wzór. Aby znaleźć liczbę neutronów w przyszłości, użyj tego wzoru: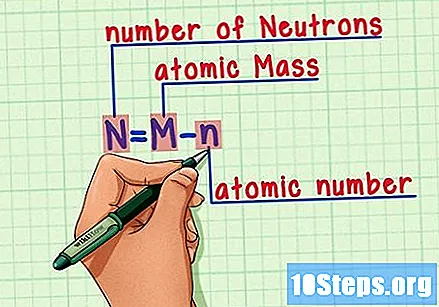
- N = M - n.
- N = liczba Neutrony.
- M = Matomowa pieczeń.
- n = natomowa kość ramienna.
- N = M - n.
Porady
- Osm, metal w stanie stałym w temperaturze pokojowej, wywodzi swoją nazwę od greckiego słowa oznaczającego „zapach”, „osme”.
- Protony i neutrony stanowią prawie całą masę pierwiastków, podczas gdy elektrony i inne różnorodne cząstki reprezentują znikomą masę (zbliżającą się do masy zerowej). Ponieważ proton ma mniej więcej taką samą wagę jak obojętny, a liczba atomowa reprezentuje liczbę protonów, możemy po prostu odjąć liczbę protonów od masy całkowitej.
- Jeśli nie masz pewności, która liczba jest która w układzie okresowym, pamiętaj, że zwykle składa się ona z liczby atomowej (to znaczy liczby protonów), która zaczyna się od 1 (wodór) i rośnie o jedną jednostkę na od lewej do prawej, kończąc na 118 (Ununóctio). Dzieje się tak, ponieważ liczba protonów w atomie określa, czym jest ten atom, ułatwiając uporządkowanie charakterystyki elementarnej (na przykład atom z 2 protonami zawsze będzie helem, tak jak inny atom z 79 protonami zawsze będzie złotem).