Autor:
Mike Robinson
Data Utworzenia:
7 Wrzesień 2021
Data Aktualizacji:
11 Móc 2024

Zawartość
Liczba atomowa odpowiada liczbie protonów w jądrze pojedynczego atomu pierwiastka. Ta wartość się nie zmienia; dlatego możesz go użyć do odkrycia innych cech izotopu, takich jak liczba neutronów.
Kroki
Część 1 z 2: Znajdowanie liczby atomowej
Znajdź kopię układu okresowego. Kliknij tutaj, jeśli nie masz takiego dostępnego. Każdy pierwiastek ma własną liczbę atomową; w związku z tym nie ma skrótów do nauki treści. Użyj kopii tabeli lub spróbuj ją zapamiętać.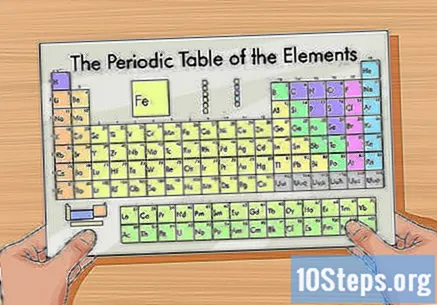
- Większość książek o chemii ma tabelę wydrukowaną na tylnej okładce.

Znajdź w tabeli element, którego się uczysz. Większość tabel zawiera pełne nazwy pierwiastków, a także ich symbole (na przykład Hg dla rtęci). Jeśli nie możesz znaleźć tego, czego szukasz, przejdź do trybu online i wyszukaj termin „symbol chemiczny” oraz nazwę pierwiastka.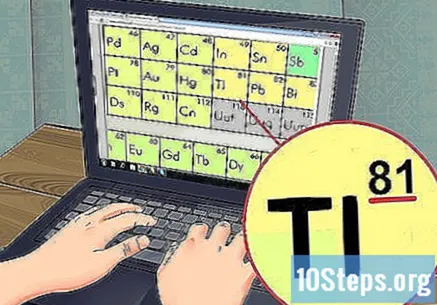
Znajdź liczbę atomową pierwiastka. Zwykle znajduje się w lewym lub prawym górnym rogu domu elementu, ale może też pojawić się w innych miejscach. Ponadto jest to zawsze liczba całkowita.- Jeśli liczba zawiera kropkę dziesiętną, prawdopodobnie oznacza masę atomową.
Potwierdź informacje zgodnie z elementami w pobliżu. Układ okresowy jest uporządkowany według kolejności liczb atomowych. Jeśli na przykład liczba izotopów wynosi „33”, pierwiastek po lewej stronie będzie miał wartość „32”, a ten po prawej stronie - „34”. W takim przypadku to dlatego, że patrzysz na liczbę atomową.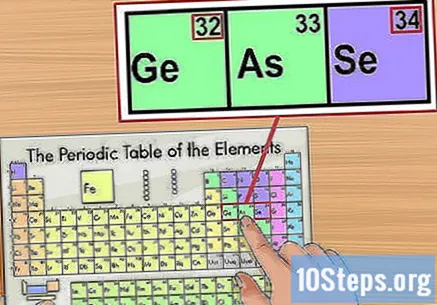
- Jest przeskok między elementami „56” (bar) i „88” (radio). Izotopy odpowiadające temu zakresowi znajdują się w dwóch wierszach poniżej tabeli. Są rozdzielane tylko w ten sposób, aby stół nie był zbyt duży.
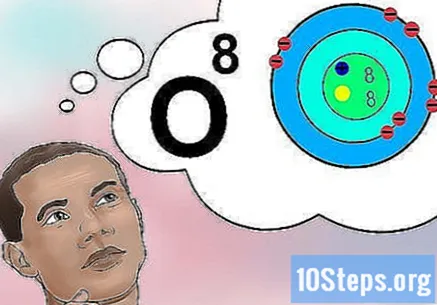
Zrozum, co oznacza liczba atomowa. Liczba atomowa ma prostą definicję: ilość protonów w atomie pierwiastka. Ta ilość protonów z kolei determinuje całkowity ładunek elektryczny jądra - który w konsekwencji określa, ile elektronów może naładować atom. Ponieważ elektrony są odpowiedzialne za prawie wszystkie oddziaływania chemiczne, liczba atomowa wpływa pośrednio na właściwości fizyczne i chemiczne pierwiastka.- Innymi słowy, każdy atom z ośmioma protonami odpowiada atomowi tlenu. Dwa atomy tlenu mogą mieć różną liczbę neutronów lub (jeśli jeden jest jonem) lub elektronów, ale każdy z nich zawsze będzie miał osiem protonów.
Część 2 z 2: Odkrywanie ważniejszych informacji
Określ masę atomową. Zwykle występuje pod nazwą pierwiastka w układzie okresowym i ma dwa lub trzy miejsca po przecinku. Masa atomowa odpowiada średniej masie atomów pierwiastka, co oznacza, że występuje on w przyrodzie. Jest mierzona w „atomowych jednostkach masy” („u” lub „u.m.a”).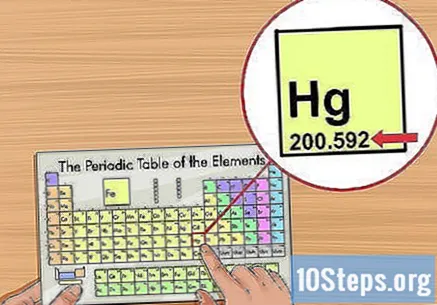
- Wielu naukowców woli używać terminu „masa atomowa” zamiast masy.
Zrozumieć masę atomową. Pojęcie masy atomowej jest bardzo podobne do pojęcia wagi. Różnica polega na tym, że waga wskazuje średnią masę dowolnego atomu w elemencie, a nie konkretny atom. Na przykład: gram żelaza zawiera kilka atomów o różnych masach; waga wskazuje na ich „masę względną”. Jeśli badasz pojedynczy atom pierwiastka, wystarczy znać jego masę.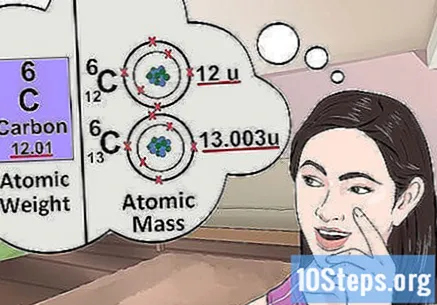
- Ogólnie, problemy chemiczne dotyczące samych atomów już wpływają na liczbę mas atomowych. Musisz tylko zrozumieć koncepcję, aby nie dać się zaskoczyć, gdy zobaczysz inną wartość.
Zaokrąglij liczbę masową. Liczba masowa odpowiada całkowitej ilości protonów i neutronów w atomie pierwiastka. Nie jest trudno to obliczyć: wystarczy wziąć masę atomową wydrukowaną w układzie okresowym i zaokrąglić ją do najbliższej wartości całkowitej.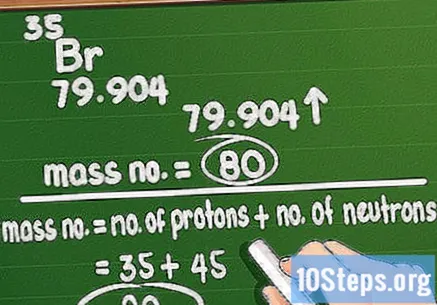
- To działa, ponieważ ilość neutronów i protonów jest bardzo bliska 1 u.m.a., podczas gdy ilość elektronów jest bardzo bliska zeru. Masa atomowa wymaga dokładnych obliczeń w celu określenia wartości dziesiętnej, ale jedynymi danymi, które mają znaczenie, są liczby całkowite, które mówią, ile jest protonów i neutronów.
- Pamiętaj, że jeśli używasz masy atomowej, będziesz bałaganić wagę konkretnego atomu w elemencie. Na przykład próbka bromu ma masę atomową 79 lub 81.
Oblicz liczbę neutronów. Teraz już wiesz, że liczba atomowa jest równa liczbie protonów, a liczba masowa jest równa sumie liczby protonów i neutronów. Aby określić ilość neutronów w pierwiastku, po prostu odejmij liczbę atomową od całkowitej masy. Kilka przykładów:
- Atom helu (He) ma liczbę masową 4 i liczbę atomową 2. Zatem 4 - 2 = 2 neutrony.
- Próbka srebra (Ag) ma średnią liczbę masową 108 (według układu okresowego) i liczbę atomową 47. Średnio każdy atom w próbce ma 108 - 47 = 61 neutronów.
Zrozum izotopy. Izotop to specyficzna forma pierwiastka, która zawiera pewną liczbę neutronów. Jeśli problem, który chcesz rozwiązać, przynosi coś takiego jak "bor-10" lub "B", to dlatego, że mówisz o pierwiastkach boru o liczbie masowej 10. Użyj tej wartości, a nie "normalnych" wartości borowy.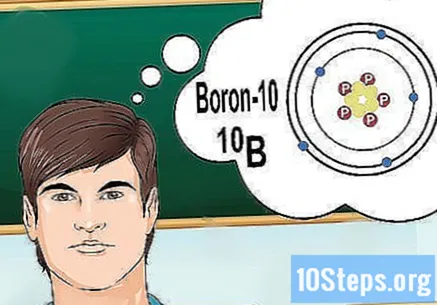
- Liczba atomowa izotopów nigdy się nie zmienia. Każdy izotop pierwiastka ma taką samą liczbę protonów.
Porady
- Masę atomową niektórych cięższych pierwiastków podano w nawiasach lub kwadratowych. Oznacza to, że ta waga jest dokładną masą najbardziej stabilnego izotopu, a nie średnią kilku izotopów. Wreszcie nie wpływa to na liczbę atomową pierwiastka.